 이미지 확대보기
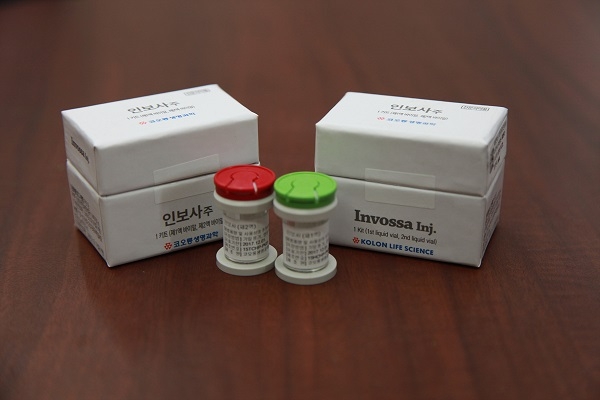
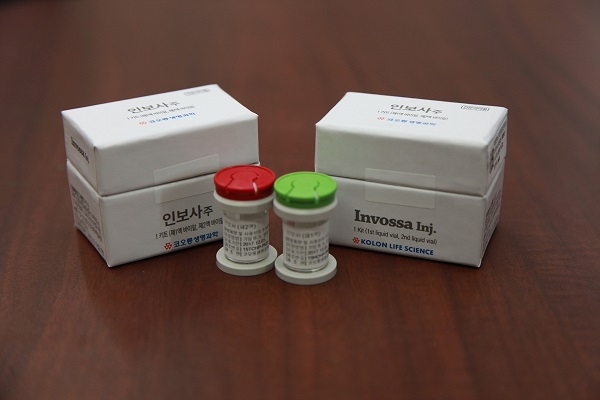
이미지 확대보기코오롱티슈진은 이미 2015년 5월에 임상 3상 계획을 미국 FDA로부터 승인받고 임상시료 사용 허가를 받기 위한 공정을 진행해왔다.
인보사의 미국 임상 3상은 약 1020명의 환자를 대상으로 50여 개 이상의 임상기관에서 진행될 예정이다. 코오롱티슈진은 임상병원과의 계약, 각 병원의 임상시험심사위원회와 임상 절차와 협의가 마무리되는 시점에서 임상환자의 등록과 투여를 시작할 수 있을 것으로 보고 있다.
이범섭 코오롱티슈진 이범섭 대표이사는 “이번 美FDA의 결정으로 인보사의 최종 품목허가 승인을 향해 한 걸음 더 나아갈 수 있게 됐다”며 “임상 3상을 성공적으로 수행해 전 세계 골관절염 환자들에게 치료제를 공급할 계획이다”라고 밝혔다.
오소영 기자 osy@g-enews.com